La estructura atómica es uno de esos temas que, a primera vista, puede parecer un poco intimidante. Pero, ¡no te preocupes! Vamos a desglosarlo y hacerlo mucho más accesible. Imagina que el átomo es como una pequeña ciudad, donde cada parte tiene un papel específico que desempeñar. En esta «ciudad», los protones y neutrones son los habitantes del núcleo, mientras que los electrones giran alrededor como turistas curiosos. ¿No es fascinante pensar que todo lo que vemos a nuestro alrededor, desde un simple grano de arena hasta un majestuoso elefante, está compuesto por estas diminutas ciudades atómicas? A lo largo de la historia, varios científicos han contribuido a nuestra comprensión de esta estructura, y hoy vamos a explorar esos hitos clave.
El viaje hacia el descubrimiento de la estructura atómica no fue fácil. A medida que los científicos comenzaban a formular teorías sobre la materia, se dieron cuenta de que necesitaban un modelo más sólido para explicar lo que veían. Desde la antigua Grecia, donde filósofos como Demócrito propusieron que todo estaba hecho de pequeñas partículas indivisibles, hasta los modernos modelos cuánticos, cada descubrimiento ha sido un paso crucial. En este artículo, nos adentraremos en los principales avances en la teoría atómica, analizando cómo cada uno de ellos ha moldeado nuestra comprensión actual de la materia.
Los Primeros Pasos: De la Teoría de los Elementos a la Atómica
La historia de la estructura atómica comienza en la antigua Grecia, donde filósofos como Demócrito y Epicuro propusieron que la materia estaba compuesta de partículas diminutas llamadas átomos. Sin embargo, fue en el siglo XIX cuando la ciencia comenzó a tomar un rumbo más experimental. John Dalton, un químico inglés, propuso la primera teoría atómica moderna en 1803. Dalton argumentó que los átomos eran esferas indivisibles que se combinaban en proporciones específicas para formar compuestos. Su teoría fue revolucionaria, ya que proporcionó un marco para entender la composición de la materia.
Los Avances de J.J. Thomson
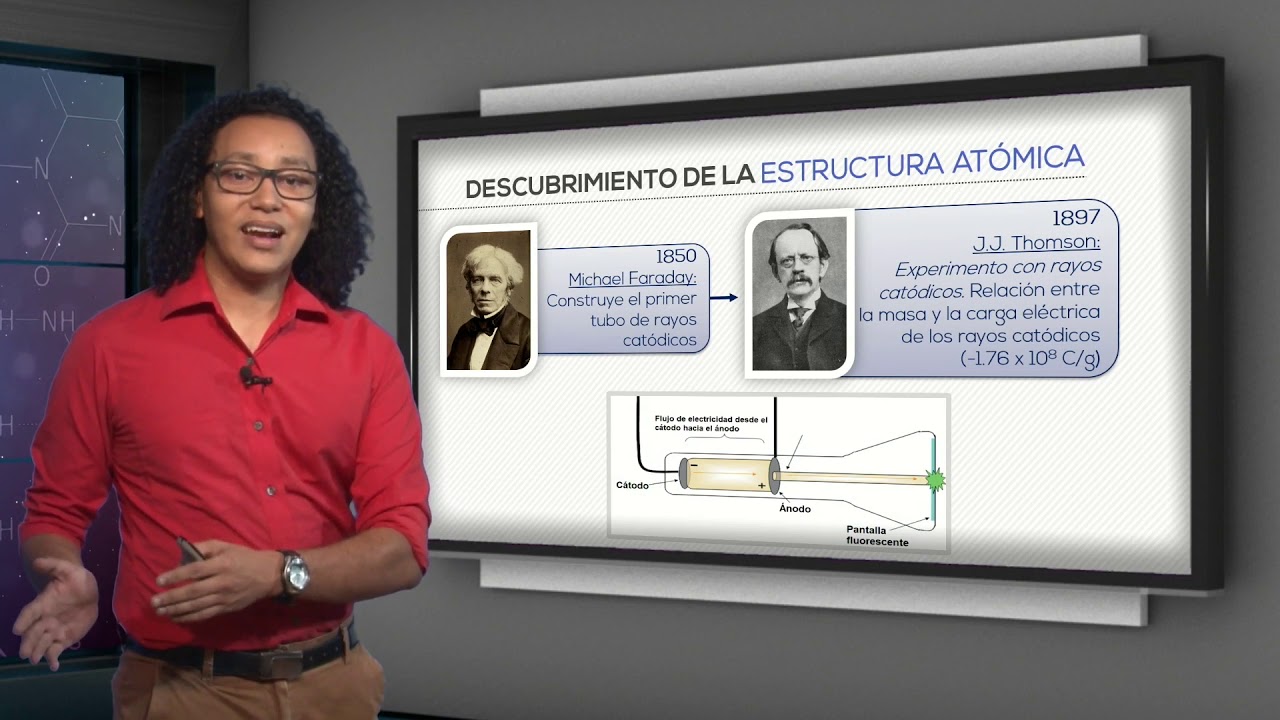
La historia dio un giro significativo a finales del siglo XIX con J.J. Thomson y su famoso experimento con el tubo de rayos catódicos. ¿Te imaginas ser capaz de «ver» átomos? Aunque no exactamente, Thomson logró demostrar que los átomos no eran indivisibles, como se pensaba. En 1897, descubrió el electrón, una partícula subatómica cargada negativamente. Este descubrimiento llevó a la creación del modelo «pudín de ciruelas», donde los electrones estaban incrustados en una esfera positiva, similar a las ciruelas en un pudín. Aunque este modelo no era perfecto, fue un gran paso hacia la comprensión de la estructura atómica.
El Núcleo Atómico: El Descubrimiento de Ernest Rutherford
Si el modelo de Thomson fue un avance, el de Ernest Rutherford en 1911 fue una revolución. Rutherford llevó a cabo su famoso experimento de la lámina de oro, donde bombardeó una delgada lámina de oro con partículas alfa. Lo que encontró fue sorprendente: la mayoría de las partículas pasaban a través de la lámina, pero algunas se desviaban en ángulos extraños. Esto le llevó a concluir que el átomo no era solo una esfera de carga positiva, sino que tenía un núcleo denso y cargado positivamente en su centro. Imagínate que el átomo es como un sistema solar, donde el núcleo es el sol y los electrones son los planetas girando a su alrededor.
El Modelo de Bohr: Un Paso Más Cerca de la Verdad
Luego, en 1913, Niels Bohr propuso un modelo que incorporaba la teoría cuántica. Según Bohr, los electrones no solo giran alrededor del núcleo, sino que lo hacen en órbitas específicas o niveles de energía. Este modelo explicó cómo los electrones podían saltar entre niveles de energía al absorber o emitir energía. Imagina que los electrones son como bailarines en un escenario, moviéndose entre diferentes niveles de luz. Este modelo fue fundamental para entender la espectroscopía y cómo los átomos interactúan con la luz.
La Teoría Cuántica y el Modelo Moderno
A medida que avanzaba el siglo XX, la teoría cuántica comenzó a jugar un papel crucial en nuestra comprensión de la estructura atómica. Los físicos como Werner Heisenberg y Erwin Schrödinger contribuyeron a desarrollar un modelo más sofisticado. En lugar de ver a los electrones como partículas que siguen trayectorias definidas, comenzaron a describirlos como nubes de probabilidad. Esta idea revolucionó la física, sugiriendo que, en lugar de saber exactamente dónde está un electrón, solo podemos calcular la probabilidad de encontrarlo en un lugar determinado.
La Dualidad Onda-Partícula
Una de las ideas más intrigantes de la teoría cuántica es la dualidad onda-partícula. Esta teoría establece que las partículas subatómicas, como los electrones, pueden comportarse tanto como partículas como ondas. Es como si tuvieras un amigo que, dependiendo del día, puede ser un excelente bailarín o un gran cantante. En el mundo cuántico, esta dualidad es fundamental para entender cómo funcionan los átomos y cómo interactúan entre sí.
La Física de Partículas: Más Allá del Átomo
A medida que la investigación avanzaba, los científicos comenzaron a explorar más allá de los átomos. La física de partículas se convirtió en un campo emocionante, donde se estudian las partículas fundamentales que componen los átomos: quarks y leptones. El descubrimiento del bosón de Higgs en 2012 fue un hito monumental, confirmando la existencia de la partícula responsable de dar masa a otras partículas. Este descubrimiento no solo profundizó nuestra comprensión de la materia, sino que también abrió la puerta a nuevas preguntas sobre el universo.
Las Implicaciones de la Estructura Atómica
La comprensión de la estructura atómica no solo ha cambiado la física, sino que ha tenido un impacto profundo en diversas áreas, como la química, la biología y la tecnología. Desde el desarrollo de nuevos materiales hasta avances en medicina y energía, el estudio de los átomos y sus interacciones ha sido fundamental. Piensa en cómo la tecnología moderna, como los teléfonos inteligentes y los dispositivos médicos, depende de nuestra comprensión de la materia a nivel atómico.
El Futuro de la Investigación Atómica
Entonces, ¿qué nos depara el futuro en el estudio de la estructura atómica? La ciencia sigue avanzando, y con ello, nuestras preguntas se vuelven más complejas. ¿Cómo podemos manipular átomos y moléculas para crear nuevos materiales? ¿Qué secretos nos revelará la física cuántica sobre la naturaleza del universo? La investigación en áreas como la computación cuántica y la nanotecnología está en auge, y promete revolucionar nuestra forma de entender y utilizar la materia.
En resumen, el descubrimiento de la estructura atómica ha sido un viaje fascinante que abarca siglos de exploración y descubrimiento. Desde las ideas iniciales de los filósofos griegos hasta los modernos avances en física cuántica, cada paso ha sido crucial para entender el mundo que nos rodea. ¿Te has preguntado alguna vez cómo estas pequeñas «ciudades» atómicas afectan tu vida diaria? Desde la comida que comes hasta la tecnología que usas, todo está conectado a la estructura atómica.
- ¿Quién fue el primero en proponer la teoría atómica moderna?
John Dalton fue el pionero en proponer la teoría atómica moderna a principios del siglo XIX. - ¿Qué descubrió J.J. Thomson?
Thomson descubrió el electrón en 1897, desafiando la idea de que los átomos eran indivisibles. - ¿Qué es el modelo de Bohr?
El modelo de Bohr describe a los electrones orbitando el núcleo en niveles de energía específicos. - ¿Qué es la dualidad onda-partícula?
Es la idea de que las partículas subatómicas pueden comportarse tanto como partículas como ondas. - ¿Cuál es el futuro de la investigación atómica?
El futuro incluye avances en computación cuántica, nanotecnología y nuevas formas de manipular átomos.